超分辨荧光显微成像技术打破了光学衍射极限的桎梏,使人类得以用无损的方式窥探纳米尺度的微观生物世界,为人类探索生命的奥秘提供了前所未有的手段。其中,超分辨结构光照明显微镜(super-resolution structured illumination microscopy, SR-SIM)具有更快的成像速度、更低的光毒性以及更弱的光漂白,在活体细胞的长时间动态观测中备受青睐。然而,在进行活细胞成像时,背景荧光不仅会导致SR-SIM图像对比度急剧下降,同时还会产生大量周期性的计算伪影,为分辨活细胞中的精细结构带来了巨大的挑战。同时,传统SR-SIM复杂、耗时的重构算法使得实现实时的超分辨观测变得困难重重。通常情况下,SR-SIM用户必须首先使用宽场模式搜索感兴趣的视场,然后切换到SR-SIM模式采集原始SIM图像,接着将SIM原始图像导入图像后处理程序,等待程序完成图像重建,最后才能观察到样品的超分辨图像。这种繁琐的工作流程对于显微镜操作者来说无疑十分低效,不可避免地阻碍了SR-SIM在生物学实验室中的广泛应用。
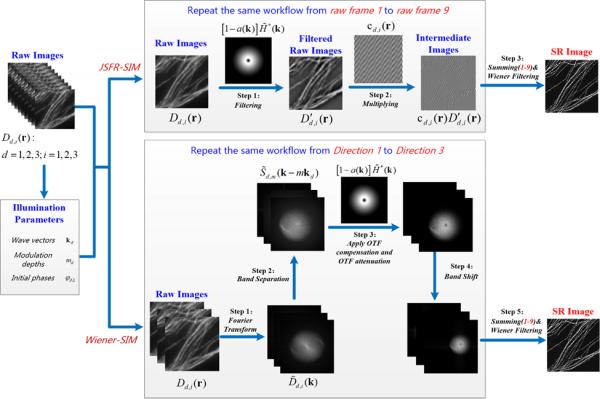
传统Wiener-SIM算法和JSFR-SIM算法重建流程对比示意图
雷铭教授团队提出了一种空频域混合式重建算法(Joint Space and Frequency Reconstruction, JSFR-SIM),极大地提高了SR-SIM的图像重建速度,解决了传统重建方法难以实现实时重建的问题。同时,该算法还能够有效抑制活细胞成像时的背景荧光与周期性的计算伪影,为解析活细胞中细胞器的精细结构观测提供了极大的便利。经测试,该方法将SR-SIM的图像重建时间缩短到毫秒级别并实现了超分辨图像的实时显示,重建速度比目前广泛使用的Wiener-SIM算法快了近2个数量级。理论模拟和实验观测均证明该方法在提升重建速度的同时并不会损失任何图像质量。
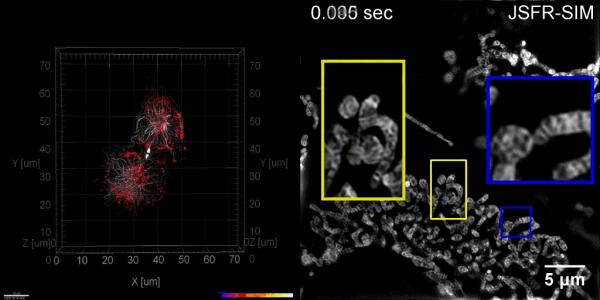
JSFR-SIM可实时显示微管和线粒体动态
另外,雷铭教授团队还将该算法与自行研制的超分辨结构光照明显微镜结合,对活体COS-7细胞进行了实时观测,并捕捉到了微管的动态组装与解体过程以及快速的线粒体制管过程。该方法为实时观察活细胞中细胞器与生物大分子的动态过程提供了一种快速的重建手段,有望大幅简化超分辨显微镜使用者的工作流程,提高相关科学工作者的成像效率,从而促进SR-SIM在生物医学实验室的广泛应用。相关技术目前已授权和正在申请多项国家发明专利,系统工程样机也已经研制完成。

快速实时超分辨结构光照明显微成像系统原理样机
相关研究成果日前以《超分辨结构光照明显微图像的高速重构》(High-speed image reconstruction for optically sectioned, super-resolution structured illumination microscopy)为题,在线发表于中国激光杂志社与国际光学工程学会(SPIE)联合创办的高起点新刊《先进光子学》(Advanced Photonics)。论文的第一单位为西安交通大学,第一作者为新讲师汪召军博士,通讯作者为雷铭教授。此外,物理学院博士后赵天宇、北京大学生命学院博士后蒿慧文等也参与了研究工作。研究工作得到了国家自然科学基金重点项目、西安交通大学中央高校建设世界一流大学(学科)和特色发展引导专项资金、西安交通大学青年拔尖人才计划项目、陕西省重点科技创新团队项目的支持。
雷铭教授团队长期从事超分辨光学显微成像技术及其在生物学中的应用研究,所研制的结构光照明超分辨显微镜具有国际领先水平,与国内外多家科研机构开展了研究合作。团队2021年获批“先进光学成像融合人工智能”陕西省重点科技创新团队。
论文链接:https://doi.org/10.1117/1.AP.4.2.026003
雷铭教授团队主页:http://gr.xjtu.edu.cn/web/ming.lei